Yazar:
Mike Robinson
Yaratılış Tarihi:
7 Eylül 2021
Güncelleme Tarihi:
11 Mayıs Ayı 2024

İçerik
Atom numarası, bir elementin tek bir atomunun çekirdeğindeki proton sayısına karşılık gelir. Bu değer değişmez; bu nedenle, izotopun nötron sayısı gibi diğer özelliklerini keşfetmek için kullanabilirsiniz.
Adımlar
Bölüm 1/2: Atom Numarasını Bulmak
Periyodik tablonun bir kopyasını bulun. Elinizde yoksa burayı tıklayın. Her elementin kendi atom numarası vardır; bu nedenle, içeriği öğrenmek için hiçbir kısayol yoktur. Tablonun bir kopyasını kullanın veya ezberlemeye çalışın.
- Çoğu kimya kitabının arka kapağında tablo basılıdır.

Tabloda incelediğiniz öğeyi bulun. Tabloların çoğu, öğelerin tam adlarının yanı sıra sembollerini de içerir (örneğin cıva için Hg). Aradığınızı bulamazsanız, çevrimiçi olun ve "kimyasal sembol" terimleri ve elementin adıyla bir arama yapın.
Elementin atom numarasını bulun. Genellikle elemanın evinin sol veya sağ üst köşesinde bulunur, ancak başka yerlerde de gelebilir. Ek olarak, her zaman bir tamsayı değeridir.- Sayı bir ondalık nokta içeriyorsa, muhtemelen atomik kütleyi gösterir.
Bilgileri yakındaki unsurlara göre onaylayın. Periyodik tablo, atom numaralarının sırasına göre düzenlenmiştir. İzotop numaranız "33" ise, örneğin soldaki öğe "32" ve sağdaki öğe "34" olacaktır. Bu durumda, atom numarasına baktığınız içindir.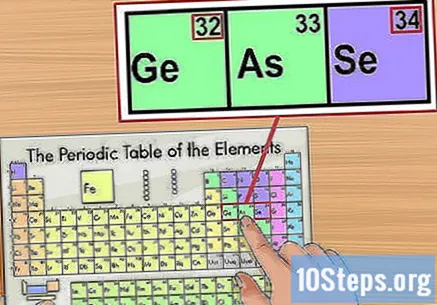
- "56" (baryum) ve "88" (radyo) öğeleri arasında bir sıçrama var. Bu aralığa karşılık gelen izotoplar, tablonun altındaki iki sıradadır. Sadece bu şekilde ayrılırlar, böylece masa çok büyük olmaz.
Atom numarasının ne anlama geldiğini anlayın. Atom numarasının basit bir tanımı vardır: elementin bir atomundaki proton miktarı. Bu miktardaki proton, çekirdeğin toplam elektrik yükünü belirler - bu da sonuç olarak atomun kaç elektron yükleyebileceğini belirler. Elektronlar neredeyse tüm kimyasal etkileşimlerden sorumlu olduğundan, atom numarası dolaylı olarak elementin fiziksel ve kimyasal özelliklerini etkiler.- Başka bir deyişle, sekiz protonlu her atom bir oksijen atomuna karşılık gelir. İki oksijen atomunun farklı sayıda nötron veya (eğer biri bir iyonsa) veya elektron olabilir, ancak her zaman sekiz protona sahip olacaklardır.
Bölüm 2/2: Daha önemli bilgileri keşfetme
Atom ağırlığını belirleyin. Genellikle periyodik tablodaki elementin adı altında gelir ve iki veya üç ondalık basamağı vardır. Atom ağırlığı, doğada nasıl bulunduğunu temsil eden bir elementin atomlarının ortalama kütlesine karşılık gelir. "Atomik kütle birimleri" ("u" veya "u.m.a") cinsinden ölçülür.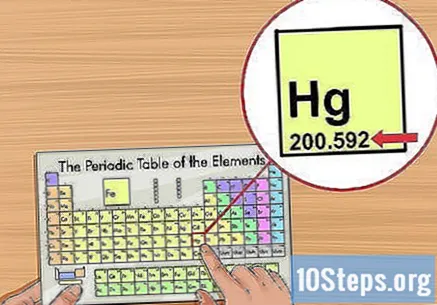
- Pek çok bilim adamı ağırlık yerine "atomik kütle" terimini kullanmayı tercih ediyor.
Atomik kütleyi anlayın. Atomik kütle kavramı, ağırlık kavramına çok benzer. Aradaki fark, ağırlığın belirli bir atomu değil, elementteki herhangi bir atomun ortalama kütlesini göstermesidir. Örneğin: bir gram demir, değişen kütlelere sahip birkaç atom içerir; ağırlık, "göreli kütlelerini" belirtir. Eğer elementin tek bir atomunu incelerseniz, sadece belirli kütlesini bilmeniz gerekir.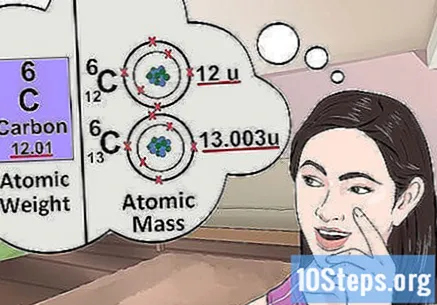
- Genel olarak, tek başına atomları içeren kimya problemleri atomik kütle numarasını zaten bildirir. Farklı bir değer gördüğünüzde hazırlıksız yakalanmamak için kavramı anlamanız yeterlidir.
Kütle numarasını yuvarlayın. Kütle numarası, elementin bir atomundaki toplam proton ve nötron miktarına karşılık gelir. Hesaplamak zor değil: Periyodik tabloda basılı olan atomik kütleyi alın ve en yakın tam değere yuvarlayın.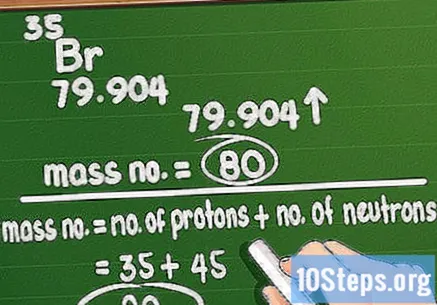
- Bu işe yarıyor çünkü nötron ve proton miktarları 1 u.m.a'ya çok yakınken, elektronlarınki ise sıfıra çok yakın. Atomik kütle, ondalık değeri belirlemek için kesin hesaplamaları içerir, ancak önemli olan tek veri, size kaç tane proton ve nötron olduğunu söyleyen tam sayılardır.
- Unutmayın, atomik kütle kullanırsanız, bir elementteki belirli bir atomun ağırlığıyla uğraşacaksınız. Örneğin bir brom numunesi, 79 veya 81 atomik kütleye sahiptir.
Nötron sayısını hesaplayın. Şimdi, atom numarasının proton sayısına eşit olduğunu ve kütle numarasının proton ve nötron sayılarının toplamına eşit olduğunu zaten biliyorsunuz. Bir elementteki nötron miktarını belirlemek için, atom numarasını o toplam kütleden çıkarmanız yeterlidir. Bazı örnekler:
- Bir helyum atomunun (He) kütle numarası 4 ve atom numarası 2'dir. Bu nedenle, 4 - 2 = 2 nötron.
- Bir gümüş (Ag) numunesinin ortalama kütle numarası 108 (periyodik tabloya göre) ve atom numarası 47'dir. Ortalama olarak, numunedeki her atom 108 - 47 = 61 nötron.
İzotopları anlayın. Bir izotop, bir dizi nötron içeren bir elementin belirli bir şeklidir. Çözmek istediğiniz problem "bor-10" veya "B" gibi bir şey getiriyorsa, bunun nedeni kütle sayısı 10 olan bor elementlerinden söz ediyor olmanızdır. "Normal" değerleri değil, bu değeri kullanın. bor.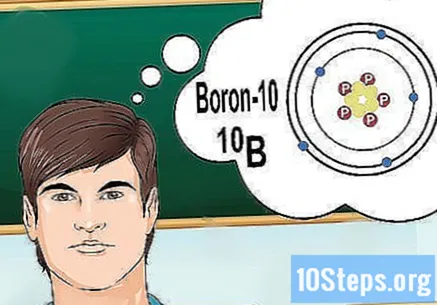
- İzotopların atom sayısı asla değişmez. Bir elementin her izotopu aynı sayıda protona sahiptir.
İpuçları
- Bazı daha ağır elementlerin atom ağırlığı parantez veya köşeli parantez içinde gelir. Bu, bu ağırlığın birkaç izotopun ortalaması değil, en kararlı izotopun tam kütlesi olduğu anlamına gelir. Son olarak, bu, elementin atom numarasını etkilemez.


